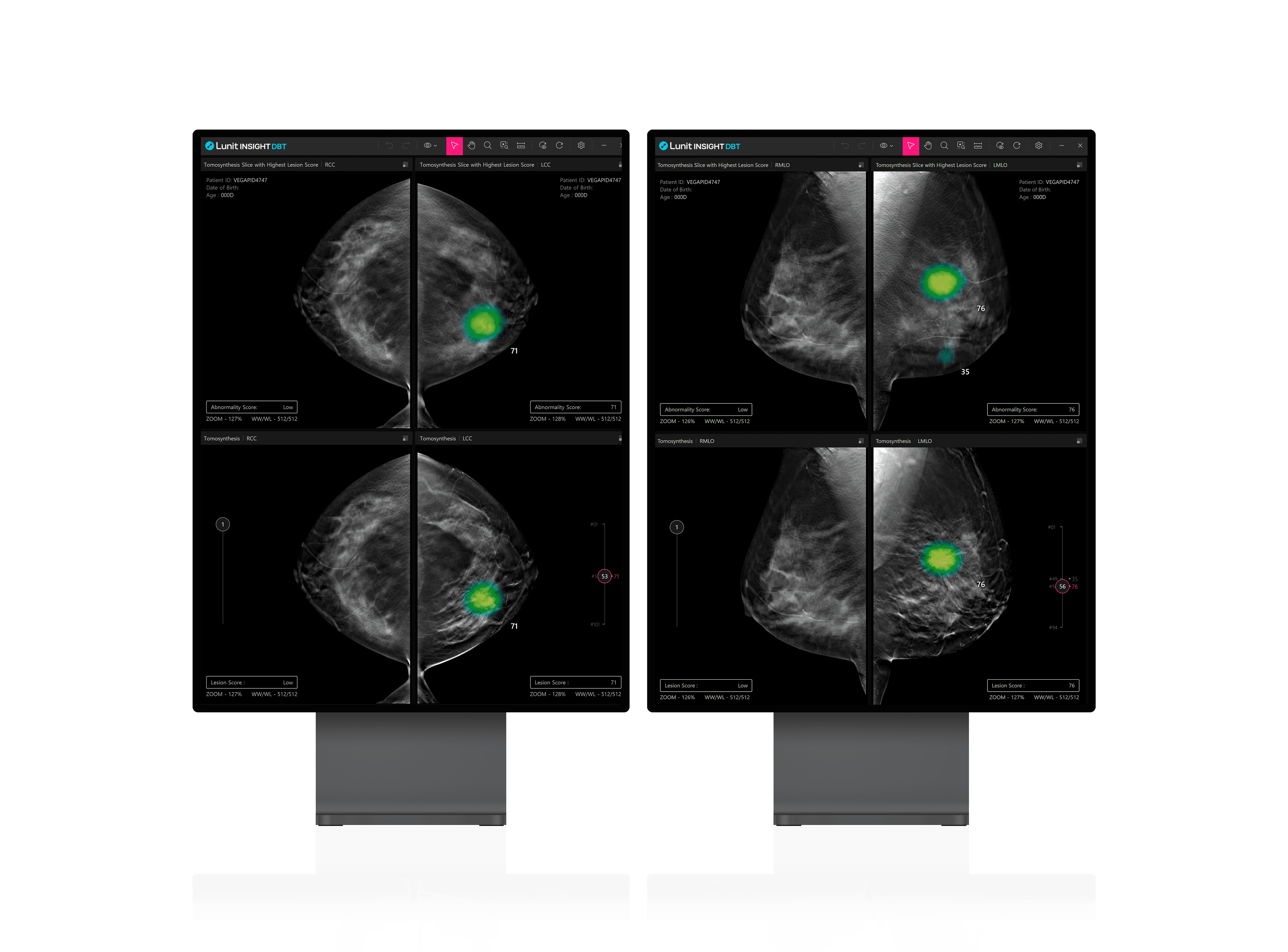
의료 인공지능(AI) 기업 루닛이 3차원(3D) 유방단층촬영술 AI 영상분석 솔루션 ‘루닛 인사이트 DBT’가 미국 식품의약국(FDA)으로부터 시판 전 허가(510(k) Clearance)를 받았다.
510(k)는 FDA가 의료기기 안전성과 유효성을 검증하는 제도로, 국내 3차원 유방암 검출 AI 솔루션이 FDA 허가를 획득한 것은 이번이 처음이다.
루닛 인사이트 DBT는 유방단층촬영술(DBT)의 3차원 영상을 AI 기반으로 분석해 의료진의 유방암 진단을 보조하는 제품이다. 특히 기존 2차원 유방촬영술에 비해 더 빠르고 정확한 진단을 제공한다는 점에서 미국 등 선진국에서 수요가 높다. 이번 FDA 인증에 따라 루닛은 미국에 본격 진출하게 됐다.
앞서 루닛은 지난 2월 유럽 자회사 ‘루닛 유럽 홀딩스’를 설립하고, 미국에 이은 거대시장 유럽에 루닛 인사이트 DBT를 출시한 바 있다. 또한 같은달 열린 유럽 최대 영상의학회 ECR 2023에서 루닛 인사이트 DBT 관련 연구가 학회 주요 연구인 구연발표(Oral PT)로 채택됐다.
서범석 루닛 대표는 “미국과 같은 의료 선진 시장에서는 이미 유방촬영술을 통한 2차원 검진을 뛰어 넘어 3차원 유방단층촬영술 방식이 대세로 자리잡았다”며 “미국 의료기관들이 유방암 정밀진단에 대한 수요가 높다는 점을 감안해 현지 의료기관을 대상으로 정확도 높은 AI 솔루션에 대한 영업·마케팅 활동을 강화하고, 시장을 신속히 확대해 나갈 것”이라고 말했다.
- 관련 기사 더보기








You must be logged in to post a comment.